溴化钠用途广泛,可用于微量测定镉,制 造溴化物。感光工业用于配制胶片感光液。医药上用于生产 利尿剂和镇静剂。香料工业中用于生产合成香料。印 染工业中用作溴化剂。此外,还用于有机合成等方面。
1 制备工艺
溴化钠的制备方法可分为中和法、还原法与离子 交换法等几种方法。目前主要的质量标准为国家化工 部标准 HG / T 3809 - 2006 标准见表 1。
项 目 | 指 标 | |
优等品 | 一等品 | |
主含量( 以 NaBr 计) 质量分数 /% ,≥ | 99. 0 | 98. 5 |
水分 /% , ≤ | 0. 3 | 0. 5 |
氯化物( 以 Cl 计) 质量分数 /% , ≥ | 0. 1 | 0. 5 |
硫酸盐( 以 SO4 计) 质量分数 /% ,≥ | 0. 01 | 0. 02 |
溴酸盐( 以 BrO3 计) 质量分数 /% ,≥ | 0. 003 | 0. 005 |
碘化物( 以 I 计) 质量分数 /% , ≥ | 0. 006 | 0. 01 |
重金属( 以 Pb 计) 质量分数 /% , ≥ | 0. 0004 | 0. 0005 |
铁( 以 Fe 计) 质量分数 /% , ≥ | 0. 0004 | 0. 0005 |
pH 值( 50g / L 溶液) | 5. 5 ~ 7. 5 | 5. 0 ~ 8. 0 |
1. 1 中和法
根据采用的原料不同,可分为两种: 一种工艺是采 用氢氧化钠与氢溴酸反应; 第二种是采用碳酸钠与氢 溴酸反应。反应过程如下( 以 NaOH 为例) : 约 40% 的 氢溴酸加入反应器中,在搅拌下缓慢加入 40% 烧碱溶液进行中和,至 pH7. 5 ~ 8 时生成溴化钠,经蒸发、结晶 再离心分离,制 得溴化钠成品。总反应方程式,方 法 ( 1) HBr + NaOH→NaBr + H2 O; 方法( 2) HBr + Na2 CO3
→NaBr + H2 O + CO2 ↑,工艺流程图见图 1( 以 NaOH 为 例) 。

中和法工艺简单,产品质量较好,但也存在缺点。 方法( 1) 采用氢氧化钠成本较高; 方法( 2) 中中和反应 放出的热量,会使溶解在氢溴酸中的溴随二氧化碳逸 出污染环境。
1. 2 尿素 还原法
尿素还原法 该工艺以溴素、碳酸钠为原料,在尿素存在的情况下还原制备溴化钠。
用纯碱和尿素在不断搅拌下溶解,然后 加入溴素,溴被还原成溴离子,与溶液中的钠离子结合 成溴化钠。溶液中的碳酸根离子和尿素反应生成二氧 化碳和氮气,从溶液中挥发出去。剩下的是溴化钠的 水溶液,蒸发后既得溴化钠产品。生产中反应温度控 制在 80℃ 左右,终止反应完成液 pH6 - 6. 5。其工艺流 程图见图 2。
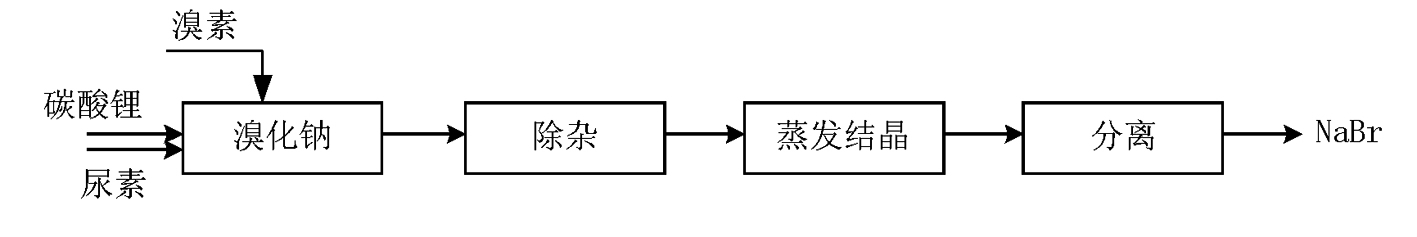
该方法因为使用溴素,所以制备过程中必须控制 温度在 80℃ 以下,否则会发生副反应,需要加入硫脲还 原。



